В этом посте, очередном из моих редких и крайне рандомных, я попробую как можно более подробно расписать все тонкости создания такой штуки как "горячий лёд" и его практическом применении. Это конечно не Гексакарбонил вольфрама какой нибудь и у любого хоть немного знакомого с химией вызовет максимум улыбку, но штука как оказалось для обывателя не менее интересная и куда как более полезная в быту.
Собственно тема варки ацетата натрия практически на кухне на пикабу уже мелькала - года четыре назад и в видеоформате от довольно годного автора, но я решил сделать версию более текстово-изобразительную с вкраплениями коротких видео (ибо гифки упорно получаются по весу раза в три толще видеоформата), которая затрагивает весь процесс целиком и полностью. Бонусом идёт несколько неочевидных нюансов поведения данной жижи в разных условиях, которые ни в каких других источниках я ни разу не видел и узнал из личного опыта возни с ней на протяжении недели.
Кому интересен непосредственно процесс кристаллизации и красивые фото можете мотать сразу на середину поста, ибо получился он у меня как всегда крайне длинным - а кому холодно и реально заняться в последующие пару дней нечем могут ознакомиться со всем процессом досконально.
Для начала немного справочной информации:
Ацетат натрия (CH3COONa), он же натриевая соль уксусной кислоты. Используется во многих отраслях производства - от химического до текстильного - в том числе пищевом как консервант под индексом E262. Но что нам интереснее всего - в качестве компонента химических обогревателей, так как при кристаллизации его водного раствора в тригидрат выделяется тепло, и выделяется его немало: ~270 кДж/кг.
И что особенно прекрасно - при нагревании выше 60°C кристаллы тригидрата ацетата натрия расплавляются обратно в свой водный раствор и остужаясь до комнатной температуры всё остаётся в таком состоянии ожидая нужного момента.
То есть можно безопасно заливать его в абсолютно любые тары превращая их в многоразовые грелки, сделать аналог 3D ручки, кристаллизировать фигурки в формочках и выращивать красивые кристаллы сколько душе угодно.
Самое интересное в данном веществе как по мне кроется в том, из чего его можно не напрягаясь сварить в ведёрке - из пачки соды, пары бутылок уксусной кислоты и небольшого количества воды. Уж этого копеечного добра точно полно если не на кухне, так в ближайшем магазине, да и процесс оказался по силе практически кому угодно.
Надеюсь со вступлением не затянул, переходим непосредственно к созданию данной жижи.
Для первого этапа синтеза самого вещества нам понадобятся:
- Гидрокарбонат натрия - обычная пачка пищевой соды на 500г
- Три флакона 70% уксусной кислоты
- Ведёрко повыше
- Черпак-мешалка
- Набор чашек и стаканов
- Шприц покрупнее (или, если имеется, поверенный мерный стакан который точно измеряет объём)
Перед началом непосредственно процесса пара советов:
1) Для начала все контейнеры очень желательно хорошо помыть и протереть, чтобы потом в готовом продукте не плавали комки пыли и волос.
2) Делать всё это лучше в проветриваемом помещении, ибо при переливании уксусная кислота нещадно выделяет разъедающие миазмы.
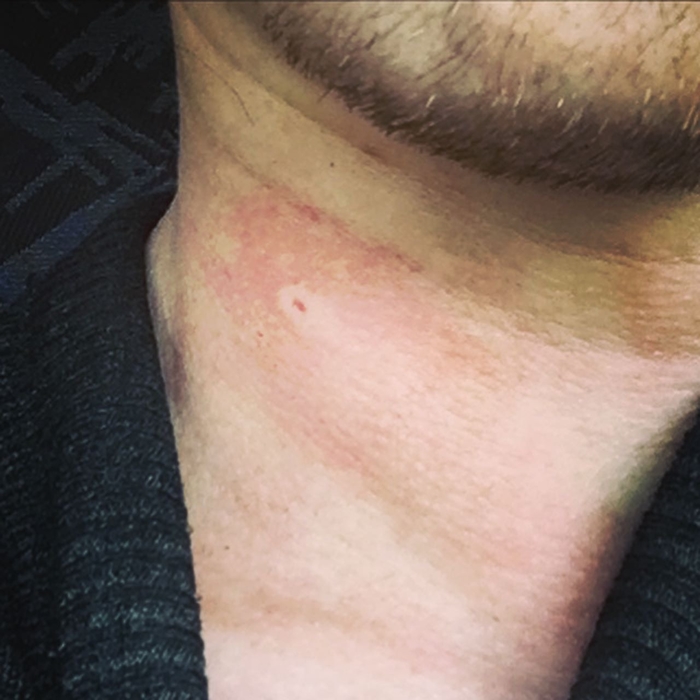
3) Вообще быть с уксусной кислотой как можно более аккуратным - она хоть и пищевая, но при достаточно длительном контакте с кожей прекрасно оставляет химические ожоги. Так что рекомендую смывать её максимально быстро.
Из видео "Огненного ТВ" идеально подошло соотношение реагентов, которое можно легко и кратно скалировать: на 500гр соды нужно 480мл уксусной кислоты и 90мл воды.
Пачку соды целиком и без лишних манипуляций высыпаем в ведро, так как там как раз 500 грамм, далее в большой стакан шприцом (да, двадцать четыре раза если он на 20мл и ничего точнее не нашлось) отмеряем кислоту и в отдельную кружку воду, желательно фильтрованную.
После чего под радостное шипение смешиваем всё это добро и наблюдаем за поднимающейся пенкой. Если брать ведро повыше то о переливании через край можно не беспокоиться - после набора определённого объёма пена схлопывается обратно с забавным звуком:
После чего остаётся только хорошо перемешать получившуюся кажу и ждать. Много ждать - около десяти-двенадцати часов, пока не закончится реакция - периодически (раз в час по началу, потом как получится) тщательно перемешивая. Пока всё это стоит и булькает лучше убрать ведёрко в хорошо проветриваемое помещение - например на балкон с любимыми цветами - и накрыть сверху чем нибудь чтобы туда не летела пыль.
Если не перемешивать, то сверху останется крайне плотная корка а внизу непрореагировавшая жидкость. Или получится как у @kirys четыре года назад: вместо снега осадок из соды, жидкость пахнущая уксусом и непонятно что делать дальше. В последнем случае, кстати, всё пошло как надо, просто жидкость не кристаллизировалась - если бы в неё кинули небольшой кристаллик ацетата натрия то через десяток секунд получился бы всё тот же самый снег.
В общем по итогу должно получиться чистое белове вещество с консистенцией мокрого снега.
Далее следует второй этап - данную кашу нужно растопить и отфильтровать от непрореагировавших компонентов и мусора.
Для этого понадобятся:
- Любая кастрюлька (за её сохранность можно не беспокоиться, всё отмывается на раз)
- Банка повыше и желательно повместительнее - та что на фото не подошла, как будет видно позже
- Воронка с любым фильтрующим материалом - бумажные полотенца вполне подходят
- Всё та же мешалка/черпалка
Снег выгружаем в кастрюльку и начинаем его топить. Делать это желательно при температуре не выше 70-80 градусов чтобы вода из раствора не слишком сильно испарялась (но долить 3-5 миллилитров воды при случае не помешает, взамен испарившейся до этого). При желании и наличии второй кастрюли побольше можно создать водяную баню и над температурой особо не раздумывать, но можно и греть просто на маленьком огне периодически перемешивая.
В итоге почти всё вещество должно раствориться в полупрозрачную маслянистую жидкость. Возможно образование кучи нерастворимой пены - её нужно вычерпать и выкинуть, но пару кусочков сохранить всё таки желательно в качестве затравки.
На втором фото видна уже подходящая для фильтрации банка:
Далее смачиваем водой фильтровальную бумагу, закладываем её в воронку и начинаем туда потихоньку переливать ещё горячую жижу. Важно чтобы она была горячей - уже остывшая она с 90% вероятностью начнёт застывать прямо в воронке. В процессе фильтрации на бумаге остаётся вся ненужная пена, осадок и прочий мусор - получается мутноватая маслянистая жидкость.
Которая после отстаивания и остывания превращается в нужную нам штуку - 0.6 литра чистого и почти полностью прозрачного водного раствора ацетата натрия, который уже можно переливать куда угодно.
К вопросу о неподходящих банках - при переливании уже остывшего ацетата в более подходящие по объёму тары будьте осторожны - кристаллизоваться эта штука начинает от малейшего намёка в виде микроскопической пылинки самого ацетата которые ты разбросал повсюду пока варил или не совсем ровного края воронки, который выступает в качестве начального центра кристаллизации. И вместо удобной для переливания жижи ты в итоге получаешь стремительно нагревающуюся банку из которой данные кристаллы вытащить уже не так просто.
Особенно сильно это доставляет когда ты только начал фильтровать, а оно уже застыло и его нужно плавить обратно.
Ну и собственно для чего всё это в основном и затевалось:
Переливаем жижу в любой удобно лежащий в руке флакончик и за копейки получаем вечную грелку для рук, которая в холода поможет быстро отогреть до онемения отмороженные руки даже на улице в любой момент. А если залить жижу в пачку от майонеза и засунуть под куртку то согреет и тушку - использование формфакторов бесконечное, а цена в ~120 рублей за целых 600мл вещества позволяет наварить его любое нужное количество. Я уже подумываю о создании саморазогревающегося жилета.
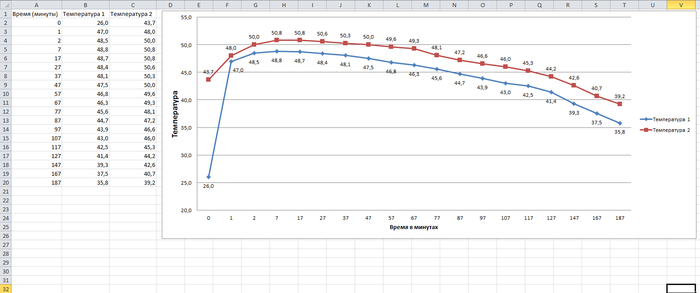
Наглядный процесс работы данной приблуды в более наглядной таре и с электронным термометром для наглядности экзотермического процесса.
Нагревается сама бутылка как раз настолько, чтобы не обжигать руки и сохраняет данную температуру до пары часов.
И чтобы впоследствии использовать грелку заново лёд из неё выковыривать не нужно - достаточно просто закинуть её в кипящую воду минут на двадцать и после остывания она снова в первозданном виде и готова к использованию. Если крышку не открывать ни для чего кроме закидывания в бутылку стартового кристалла то работать она будет вечно - нужно будет максимум раз в год долить пару миллилитров воды взамен испарившейся.
На втором фото можно увидеть примерный набор грелок из двух флакончиков и мензурки со стартовыми кристаллами
Немного красивостей - процесс кристаллизации тонкого слоя ацетата натрия на тёмной поверхности выглядит реально завораживающе.
И получившиеся в итоге кристаллы как раз можно использовать в качестве стартовых для начала кристаллизации.
Интересные факты о получающихся кристаллах - их форма и размер, как оказалось, тоже очень сильно зависят от начальной температуры жижи. Как пример: кристаллы слева получены из раствора который был охлаждён примерно до +3/+5 градусов, затвердел он крайне быстро и в итоге вещество получилось отнюдь не рассыпчатым а очень даже плотным.
А кристаллы справа росли в стакане с жижей подогретой до +40 около часа и получились крупными, рассыпчатыми и прозрачными.
Например вот этот флакончик после неравномерного разогрева в микроволновке начал кристаллизироваться когда был ещё горячим и остывал он около четырёх часов, так как выделяющееся в процессе кристаллизации тепло поддерживало критическую температуру. А кристаллы, как известно, получаются тем больше, чем более медленно они растут. В итоге в нём получилась крайне красивая гроздь крупных кристаллов - и есть у меня предположение что это далеко не предел их размерам.
На фото, кстати, процесс ещё не завершён и колбочка довольно горячая.
Напоследок несколько советов:
- Если раствор получился слишком мутным, то в растворении нерастворённого осадка может помочь миллилитр-другой уксусной кислоты - а если он слишком сильно этой самой кислотой пахнет, то отстаивание с открытой крышкой в твёрдой форме.
- Любые контактирующие с ацетатом натрия жидкой форме колбочки, крышки и палочки при нежелательности его кристаллизации крайне желательно всполаскивать в воде. Для этого же всегда закрывать крышки на банках с жижей - иначе обязательно залетит пылинка.
- Руку в банку с жижей для красивой кристаллизации вокруг ладони совать можно, но крайне осторожно и с быстрым доступом к холодной воде. Лично я пытался для красивого кадра кристаллизовать лужицу горячего льда прямо на руке и мои мёрзлые ладони этого не выдерживали - припекает в процессе будь здоров.
- После всех манипуляции все банки/столы хорошенько протереть мокрой тряпкой от остатков ацетата натрия и уксусной кислоты.
Что ж, для начала хватит, пожалуй - еле-еле вместил данный поток мысли в лимиты поста.
Экспериментируя с самими грелками в разных режимах и условиях у меня на данный момент накопилась целая пачка идей для будущих экспериментов:
1) Замерить точную тепловую динамику данных грелок в реалистичных условиях - сколько по времени они будут держать определённую температуру в холодном и разогретом до критической температуры состоянии и сравнить их динамику с бутылкой обычной горячей воды той же температуры. Благо термометр раздобыл.
2) Поэкспериментировать с механизмом запуска разогрева сравнимым с заводской грелкой - чтобы не приходилось откручивать крышку и закидывать что либо. Вариантов несколько - от сменных колпачков до залитых парафином кристаллов в гибких крышках, которые раскрываются при нажатии.
3) Попробовать использовать данную жижу в художественных целях. Например сделать панель с меняющимся при нагреве кристаллическим узором или заливать объёмные фигурки из переохлаждённого горячего льда. 3D ручка же из данного вещества получилась своеобразная - можно посмотреть на результаты в бонусном комментарии.
4) Вырастить как можно более крупный монокристал?
Если кому то будет интересен конкретный пункт или у него есть любые собственные идеи смело тыкайте в комментариях, проведу и сваяю второй пост.
P.S. - будет забавно, если в горячее выйдет пост про горячий лёд.
А баянометр показывает совсем уж странные штуки...