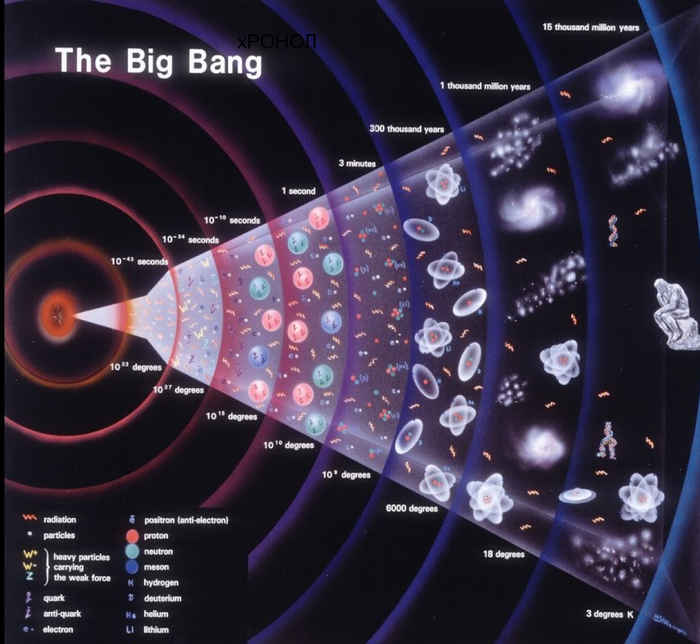
Наверное, каждый из нас, оглядываясь вокруг, задавался вопросом: А откуда это все взялось? Как мы знаем, всё состоит из атомов, все они систематизированы в Периодической таблице. Но откуда появились атомы, образующие вещества и почему одни вещества более распространены во Вселенной, чем другие. Для того, чтобы всё разобрать по порядку необходимо начать с начала, в прямом смысле этого слова, поскольку началом всего в нашей Вселенной был Большой Взрыв - момент, с которого она начала своё расширение, который, как считается, произошел 13,77 млрд. лет назад.
Начало Вселенной описывается так называемой Планковской эпохой время от 0 до 10^-43 секунд от Большого Взрыва, когда вещество Вселенной находилось в экстремальных условиях, а именно имело планковскую энергию (10^19 ГэВ), планковский радиус (10^−35 м), планковскую температуру (10^32 К) и планковскую плотность (10^97 кг/м³). В этот столь короткий промежуток времени Вселенная состояла из кварк-глюонной плазмы.
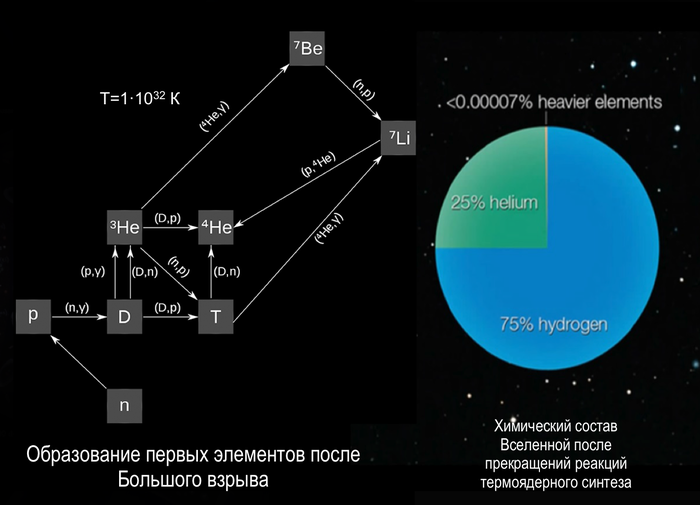
Однако уже через 10^−36 секунд температура Вселенной упала достаточно для того, чтобы сформировались протоны и нейтроны, которые в свою очередь, сталкиваясь, образовывали ядра первых атомов, а именно изотопы водорода, которые в свою очередь превращались в ядра изотопов гелия. Температура новой Вселенной продолжала падать, и атомы уже находились в устойчивом состоянии, но спустя примерно 17 минут энергии для реакции термоядерного синтеза было уже недостаточно и первый процесс образования материи из элементарных частиц завершился. Но сформированного за столь, кажется, короткое время вещества, которое распределилось по всей расширяющийся Вселенной, было достаточно для образования всего известного нам водорода и большей части гелия, из которых в последствии будут состоять звезды, являющиеся настоящими генераторами всех остальных элементов Периодической таблицы.
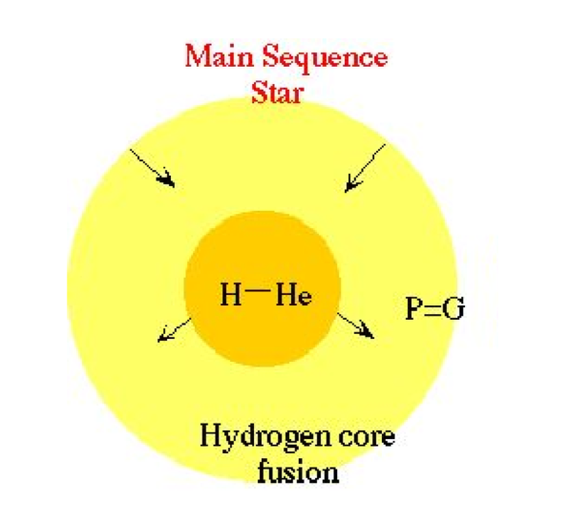
Звезды - массивные космические тела, образованные из газопылевой среды в результате гравитационного сжатия. В начале своего существования все звезды на большую часть состоят из водорода, который и расходуется на протяжении всей её жизни. Суть заключается в том, что в ядре из-за огромных давлений и температур создаются оптимальные условия для реакций термоядерного синтеза, которые происходят непрерывно, поскольку в ходе реакции из ядра во вне выделяется энергия, противостоящая силам гравитации. Таким образом, эти два процесса поддерживают звезду в равновесии.
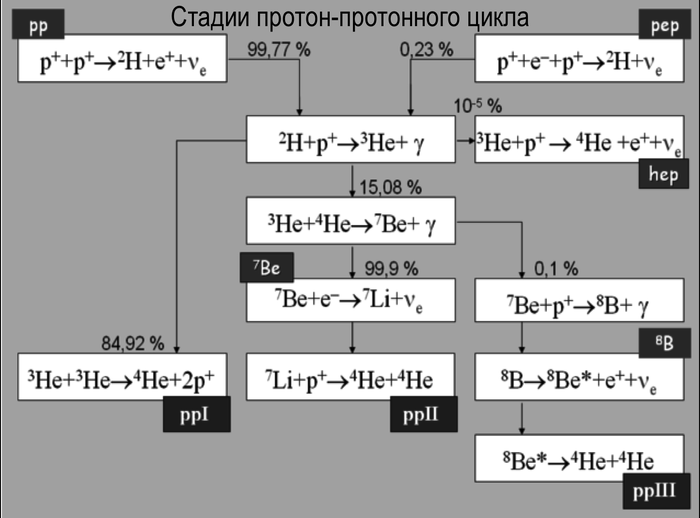
Данная совокупность термоядерных реакций в ходе которого водород превращается в гелий называется протон-протонным циклом. В ходе всего процесса выделяется свыше 18 МэВ энергии. Но это лишь один из циклов термоядерных реакций и насколько далеко может заходить синтез новых элементов зависит от массы звезды, а далее от сценария её гибели.
Причиной всего является то, что чем дальше заходит термоядерный синтез, тем больше требуется гравитационного сжатия для формирования нового элемента и тем меньше выделяется энергии. По этой причине звезды, чья масса меньше половины массы Солнца не могут расходовать на реакции гелий, когда весь водород закончится. Такие звезды принадлежат к классу красных карликов, и водород в них расходуется чрезвычайно долго. С момента зарождения Вселенной не остыл ни один красный карлик, считается, что звезда с массой 0.1 солнечной способна жить 10 триллионов лет.
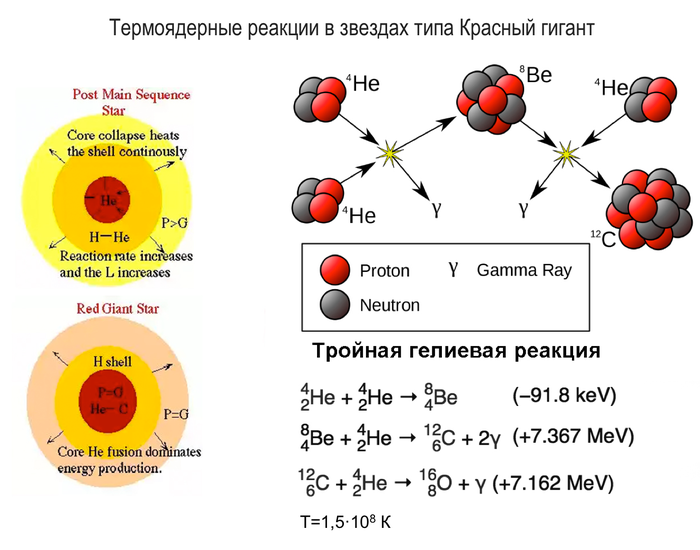
Звезды, близкие по массе к Солнцу имеют другую судьбу. Реакции термоядерного синтеза гелия из водорода происходит в течении примерно 10 млрд. лет, после чего в гелиевом ядре начинается процесс превращения его в углерод и кислород. Выделяющейся при этом энергии недостаточно, чтобы противостоять силам гравитации и внешняя оболочка звезды начинает расширяться, при этом сжимая ядро. Такие звезды называются красными гигантами и обычно не живут больше 1 миллиарда лет.
Процесс термоядерного сжигания гелия отличается от предшествующего водородного; он очень чувствителен к температуре и вызывает нестабильность в виде сильнейших пульсаций, которые сообщают внешним слоям достаточное ускорение, чтобы быть сброшенными, что в итоге и происходит.
Звезда превращается в так называемую планетарную туманность, состоящую из ионизированной газовой оболочки, выброшенной в межзвездное пространство и центра - белого карлика. Оболочка состоит из всех тех элементов, что были получены в ходе термоядерного синтеза внутри звезды (обычно это углерод, азот и кислород) и не участвовавших в реакции водорода и гелия из внешних областей бывшей звезды.
Белый карлик бывшее ядро звезды, сжатое силами гравитации до размеров Земли, но массой близкой к солнечной. В течение 50 тыс лет туманность полностью рассеивается, а белый карлик, состоящий преимущественно из гелия, который оставался в ядре звезды, постепенно охлаждается, превращаясь в черного карлика - потухшую звезду, не излучающую свет.
Однако возможен другой сценарий, при котором будут образовываться более тяжелые химические элементы. В космическом пространстве очень часто можно встретить системы из двойных звезд, например Сириус, самая яркая звезда ночного неба, на самом деле система из звезды Сириус А, немного большей в диаметре, чем Солнце и Сириуса Б - белого карлика. Белые карлики чаще всего являются компаньоном больших по размеру звезд, поскольку обладают очень высокой плотностью и силой притяжения.
По этой причине, рано или поздно белый карлик начинает забирать на себя внешнюю оболочку звезды-компаньона, из-за критических условий вновь возобновляется процесс термоядерного синтеза более тяжелых элементов - углерода, азота и кремния.
Но процесс отличается крайней нестабильностью и белый карлик не может полностью поглотить весь материал звезды-соседа. Критический момент возникает тогда, когда в ходе термоядерного синтеза появляется железо.
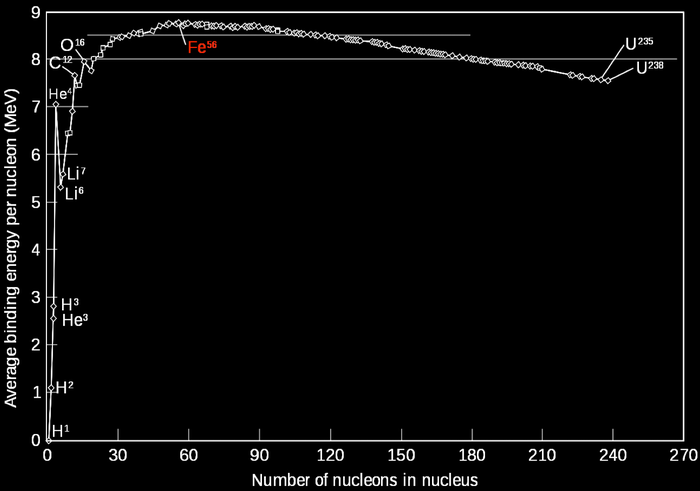
Ядро железа-56 обладает максимальным дефектом массы, вследствие чего в дальнейшем ряду прекращается выделение энергии в ходе термоядерной реакции, то есть для получения кобальта энергия уже расходуется, а не выделяется.
Когда дальнейшее превращение становится невозможным, в ядре происходит коллапс, высвобождающий такую энергию, которая буквально разрушает звезду. Этот взрыв носит название Сверхновая типа IА.
Чрезвычайная мощность взрыва разносит получившиеся в ходе синтеза химические элементы по межзвездному пространству, которые в дальнейшем образуют новые космические объекты.
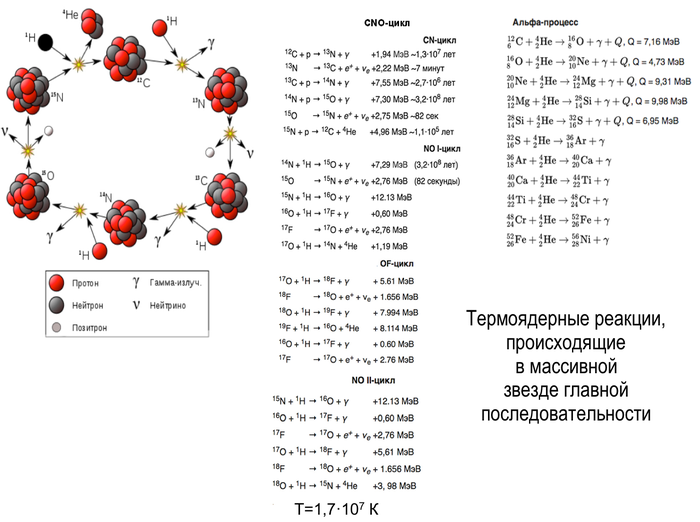
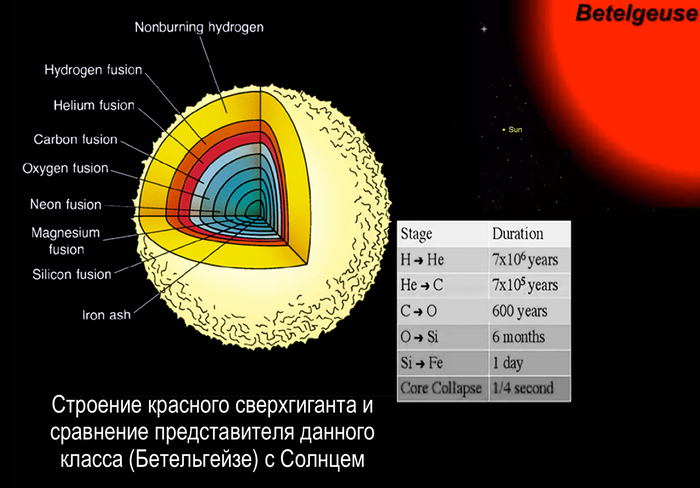
Однако железо наряду со всеми остальными не упомянутыми более тяжелыми элементами образуется в ходе финальной стадии жизненного цикла звезд, чья масса в более чем в 10 раз превышает массу Солнца. Такие звезды живут гораздо меньше, поскольку, чем больше звезды, тем более экстремальные условия возникают в ядре, и тем активнее в них идут термоядерные реакции. С исчерпанием водородного ресурса в ядре эти звезды также начинают расширяться, превращаясь в красного сверхгиганта, но огромная масса стабилизирует неустойчивое поведение гелия и в центре поддерживаются нужные условия для синтеза более тяжелых элементов, чем углерод и кислород.
Структура сверхгиганта напоминает слоеный пирог из разных элементов, которые выбрасываются из ядра во внешние слои.
Крест на всём и в этом случае ставит железо, которое начинает поглощать энергию для дальнейшего превращения, звезда выходит из состояния равновесия по действием колоссальных, гравитационных сил, которые начинают сжимать ядро до размера нескольких десятков километров. Возникающее давление настолько сильное, что между ядрами атомов не остается пустого места, а электроны сливаются с протонами, образуя нейтронную массу. Столь критические условия вызывают детонацию из самого центра звезды называемый Сверхновой типа II.
Высвобождаемая энергия вкупе с температурой в миллиарды градусов проходит через все слои сверхгиганта, в процессе чего происходит синтез всех следующих за железом элементов, и под действием невероятных сил они выбрасываются в межзвездное пространство на миллиарды километров, формируя туманность, которая будет рассеиваться еще несколько сотен тысяч лет.
Но на этом трансформация бывшего ядра не заканчивается. Если его масса была от 1.5 до 3 масс Солнца, то оно превращается в нейтронную звезду - чрезвычайно плотный объект, имеющий при данной массе диаметр 10-20 км. Обладая температурой поверхности от миллиона Кельвинов, силой магнитного поля в 100 триллионов раз больше земного и эти объекты до сих пор остаются одними из самых загадочных во Вселенной. Если ядро сверхгиганта превышало массу Солнца более чем в три раза, то оно преобразуется в еще более странный объект не подчиняющийся законом физики этой Вселенной - черную дыру. Едва ли это можно назвать объектом, скорее область в пространстве, поглощающая все частицы и волны ( в том числе свет), плотность, масса и сила притяжения которой равна бесконечности. Астрономы могут наблюдать лишь свечение от звезд, попавших в поле притяжения черной дыры или искажения более далеких объектов. До сих пор многое в особенностях черных дыр остается не изученным.
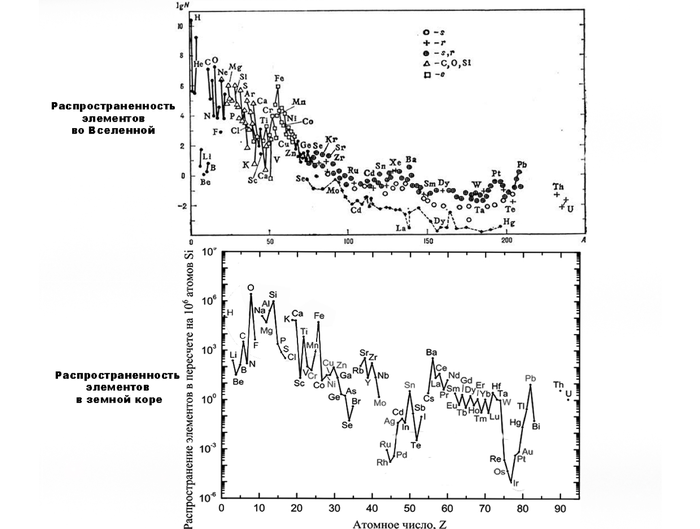
Таким образом, чем тяжелее атомное ядро элемента, тем в более экстремальных условиях космоса оно образовалось. Несмотря на то, что термоядерные реакции идут уже 13.77 млрд. лет в неисчислимом количестве звезд, доля всех остальных элементов во Вселенной не превышает одного процента. Если изобразить зависимость распространения элементов от числа их атомного номера, то получится убывающий график, при этом можно наблюдать резкий перелом сразу после железа, поскольку эти элементы образуются только в результате взрыва массивных звезд. Похожая картина наблюдается и в зависимости содержания в земной коре (кларкового числа) от атомного номера, несмотря на то, что на Земле гелия и водорода в разы меньше, и она покрыта алюмосиликатной корой, азотисто-кислородной атмосферой, а внутри имеет железо-никелевое ядро.
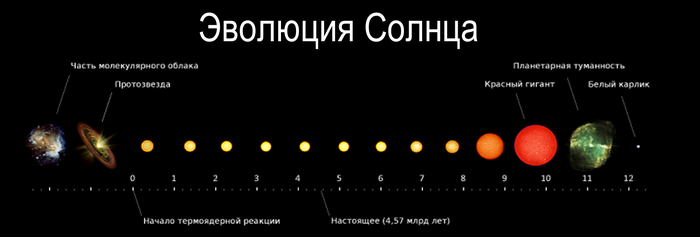
Подобный круговорот веществ всегда существовал и будет существовать в космосе, ведь в конечном итоге всё, что мы видим, превратится в пыль и осадочные породы, а через 6.5 млрд. лет Солнце, как типичная средняя звезда превратится в красного гиганта и поглотит Землю, вместе с Меркурием, Венерой и Луной, а затем сбросит оболочку и уничтожит все до орбиты Юпитера, образуя планетарную туманность с белым карликом в центре.
В дальнейшем газовые планеты будут еще несколько миллиардов лет находиться на орбите тусклой угасающей звезды, а рассеянная в космическом пространстве туманность даст жизнь другим звездам и планетам.